
Из-за блокировщика рекламы некоторые функции на сайте могут работать некорректно! Пожалуйста, отключите блокировщик рекламы на этом сайте.
Меня зовут Быстрицкая Вера Васильевна.
Вам нужны консультации по Химии по Skype?
Если да, подайте заявку. Стоимость договорная.
Чтобы закрыть это окно, нажмите "Нет".
Укажите реальные данные, иначе мы не сможем с вами связаться!
Отправляя форму, Вы принимаете Условия использования и даёте Согласие на обработку персональных данных
Отправляя форму, Вы принимаете Условия использования и даёте Согласие на обработку персональных данных





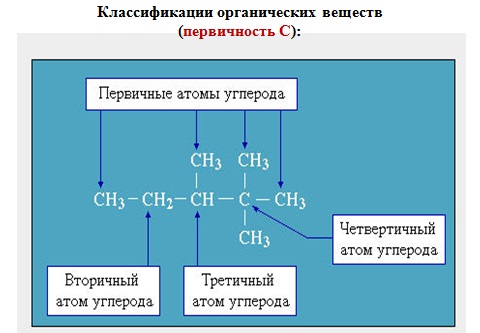
НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ ВЕЩЕСТВ
- систематическая (ИЮПАК),
- рациональная,
- тривиальная.
СИСТЕМАТИЧЕСКАЯ НОМЕНКЛАТУРА ИЮПАК (заместительная )
ИЮПАК (IUPAC ) - Международный союз теоретической и прикладной химии)
Является наиболее распространенной - в соединении выделяется некая основа, в которой произведено замещение атомов водорода на иные атомы или группы.

РАЦИОНАЛЬНАЯ НОМЕНКЛАТУРА
За основу принимают название первого члена гомологического ряда, а все остальные группы – радикалы – рассматривают как заместители. Используют в названиях простых эфиров, кетонов, аминов.

ТРИВИАЛЬНАЯ (ИСТОРИЧЕСКАЯ) НОМЕНКЛАТУРА
Возникла в начале развития органической химии, когда не существовало классификации и теории строения органических соединений.
Органическим соединениям давали случайные названия:
по источнику получения (щавелевая кислота, яблочная кислота, ванилин),
цвету или запаху (ароматические соединения),
по химическим свойствам (парафины).
Многие такие названия часто применяются до сих пор.
Например: мочевина, толуол, ксилол, уксусная кислота, масляная кислота, валериановая кислота, глицерин, этиленгликоль и многие другие.

АЛКА́НЫ (насыщенные углеводороды, парафины, алифатические соединения)
Общая формула - CnH2n+2 ( n - число атомов углерода в молекуле)
sр3-гибридизация (все атомы углерода)
все σ-связи
длина связи С-С - 0,154 нм
угол между связями С-C составляет 109°28‘ (поэтому молекулы имеют зигзагообразное строение (зигзаг).
По номенклатуре ИЮПАК в названии - суффикс –ан.
Первые четыре углеводорода носят исторически сложившиеся названия, начиная с пятого в основе названия углеводорода лежит греческое название соответствующего числа углеродных атомов.


НОМЕНКЛАТУРА АЛКАНОВ (ИЮПАК)
1. Выделяют в структурной формуле наиболее длинную цепь атомов углерода и нумеруют эти атомы, начиная с того к которому ближе радикал.
Когда радикалов несколько и они равноудалены от концов главной цепи, то нумерацию начинают с того края, к которому ближе расположен простейший радикал.

2.Записывают цифру атома углерода, у которого находится радикал, ставят тире, пишут название радикала.
Если радикалов несколько и они одинаковые, номер повторяют по числу этого радикала, а перед названием радикала приписывают приставку от греческого числительного («ди»-2, «три»-3, «тетра»-4 и т.д.).
Если радикалов несколько, и они разные, их названия записывают через тире.

3. Завершают название алкана по числу атомов углерода в нумерованной цепи.

НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
АЛКЕНЫ (олефины, этиленовые углеводороды)
Общая формула CnH2n
одна двойная связь (= ) между атомами углерода
По месту С=С - sp2 гибридизация,
угол между связями С=С - 120°, поэтому молекула угловая
одна подвижная π-связь,
длина двойной связи 0,134 нм.
НОМЕНКЛАТУРА ИЮПАК
названия алкенов производят от названий соответствующих алканов (с тем же числом атомов углерода) путем замены суффикса –ан на –ен:
2 атома С → этан → этен;
3 атома С → пропан → пропен и т.д.
У простейших алкенов наряду с -ен используется суффикс -илен: 2 атома С → этен → этилен;3 атома С → пропен → пропилен.
НОМЕНКЛАТУРА АЛКЕНОВ
1. Главная цепь обязательно включает в себя двойную связь (даже если она не самая длинная).
2. Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи.
3. Названия радикалам дается, как у алканов
4. Название главной цепи дается с суффиксом –ен, затем через тире указывается цифра, обозначающая положение двойной связи.

В номенклатуре различных классов органических соединений наиболее часто используются следующие одновалентные радикалы алкенов:

АЛКИНЫ (ацетиленовые углеводороды)
Общая формула CnH2n-2
одна тройная связь (≡).
≡ - sp-гибридизация,
≡ - одна σ- и две π-связи
угол по месту ≡ 180°, молекула линейная
длина тройной связи 0,120нм.
ИЮПАК - суффикс -ан заменяется суффиксом -ин:

НОМЕНКЛАТУРА АЛКИНОВ
Аналогична номенклатуре алкенов (суффикс –ен заменяется на суффикс -ин:

АЛКАДИЕНЫ (ДИЕНЫ, ДИЕНОВЫЕ УГЛЕВОДОРОДЫ)
Общая формула СnH2n-2
Содержат две двойные связи.
Остальные характеристики зависят от положения двойных связей
НОМЕНКЛАТУРА АЛКАДИЕНОВ
Как у алкенов (суффикс -ен меняется на суффикс -диен, указываются две цифры положения двойных связей).

По взаимному расположению двойных связей и химическим свойствам диены делятся на три группы:
1. Диены с соседним положением двойных связей называют диенами с алленовыми или кумулированными связями.
Эти соединения мало устойчивы и легко перегруппировываются в алкины, (сходны с алкинами).
Простейший представитель :

2. Диены с двойными связями, разделенными более чем одной простой связью, называются диенами с изолированными связями (сходны с алкенами):

3. Диены с 1, 3- положением двойных связей называют диенами с сопряженными связями.
Нет чисто одинарной и чисто двойных связей. Строение бутадиена более точно отражает формула с делокализованными «полуторными» связями.
Основные представители:
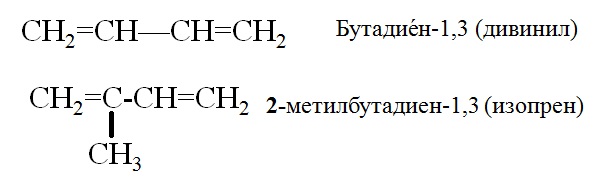
СМЕШАННЫЕ УГЛЕВОДОРОДЫ
Углеводороды две или больше тройных связей, называются алкадиинами, алкатриинами и т. д.
Углеводороды, содержащие одновременно двойные и тройные связи, называются алкенинами, алкадиенинами, алкендиинами и т. д. в соответствии с числом двойных и тройных связей.

ЦИКЛИЧЕСКИЕ УГЛЕВОДОРОДЫ Циклоалканы (нафтены, цикланы, или циклопарафины )
Общая формула СnH2n
Все атомы состоянии sp3-гибридизации
Каждый атом углерода образует четыре σ-связи С-С и С-Н.
Углы между связями зависят от размера цикла. В малых циклах С3 и С4 углы между связями С-С сильно отличаются от тетраэдрического угла 109,5°, что создает в молекулах напряжение и обеспечивает их высокую реакционную способность
НОМЕНКЛАТУРА ИЮПАК
За основу принимают углеродную цепочку цикла.
Нумерацию цикла проводят с того атома углерода, который связан с наименьшим радикалом, и продолжают в сторону ближайшего с соблюдением принципа возрастающей сложности.
Например,

При наличии радикала с длинной и разветвленной цепью за основу можно принять самую длинную открытую цепь углеродных атомов.

АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ. АРЕНЫ.
В молекулах имеется особая циклическая группировка из шести атомов углерода, называемая бензольным или ароматическим ядром.
Общая формула ароматических углеводородов CnH2n-6.
Атомы углерода в состоянии sp2-гибридизации, связан с двумя соседними атомами углерода и атомом водорода тремя σ-связями.
Валентные углы между каждой парой π-связей равны 1200.
Длина связи С–С равна 0,140 нм
Все σ-связи С–С и С–Н лежат в одной плоскости.
р-Электроны всех атомов углерода образуют единое циклическое π-электронное облако, сосредоточенное над и под плоскостью кольца.

Бензол или бензин (старинное название) С6Н6 – родоначальник ароматических углеводородов.
Все связи С–С в бензоле равноценны
Это означает, что в молекуле бензола между углеродными атомами нет чисто простых и двойных связей (как в формуле, предложенной в 1865 г. немецким химиком Ф.Кекуле),

Гомологи бензола

Радикал (остаток) бензола C6H5- носит название фенил;
Радикал C6H5-CH2-называется бензил.
Названия высших гомологов часто производят не от названия ароматического ядра, а от названия боковой цепи, т. е. их как производные алканов:

Называя более сложные производные бензола, как и в случае алициклических соединений, из возможных порядков выбирают тот, при котором сумма цифр номеров заместителей будет наименьшей.

НАЗВАНИЯ НЕКОТОРЫХ УГЛЕВОДОРОДОВ


Раздел пока пуст
-
25(П) Качественные реакции на неорганические вещества и ионы. Качественные реакции органических соединений
- Проверочный тест №1 по теме Качественные реакции на неорганические вещества и ионы
- Проверочный тест № 2 по теме Качественные реакции на неорганические вещества и ионы
- Проверочный тест №3 по теме Качественные реакции органических соединений
- Проверочный тест №4 Качественные реакции органических соединений
-
27(Б) Вычисление массы растворенного вещества, содержащегося в определенной массе раствора с известной массовой долей; вычисление массовой доли вещества в растворе.
- Проверочный тест №1 Решение задач на вычисление массы или массовой доли при изменения количества вещества или раствора
- Проверочный тест №2 Решение задач на вычисление массы или массовой доли при изменении количества вещества или воды.
- Проверочный тест №3 Решение задач на определение массовой доли при смешивании растворов с разной массовой долей растворенного вещества.
- Проверочный тест №4 Решение задач на определение массовой доли при смешивании растворов с разной массовой долей растворенного вещества.
Клиентам
Репетиторам
Партнеры

![[[pictureof]]](https://dist-tutor.info/s3/dist-tutor/user/20094/ava/thumbnails/mQ6siSVtAT1Szar.jpg)
